08-18
08-18
08-18
08-17
08-17
更新时间:2022-04-06 02:55:04作者:潘星教育网阅读量:93
08-18
08-18
08-18
08-17
08-17

高中化学教师资格面试逐字稿
1、题目:《电解池》
2、内容:
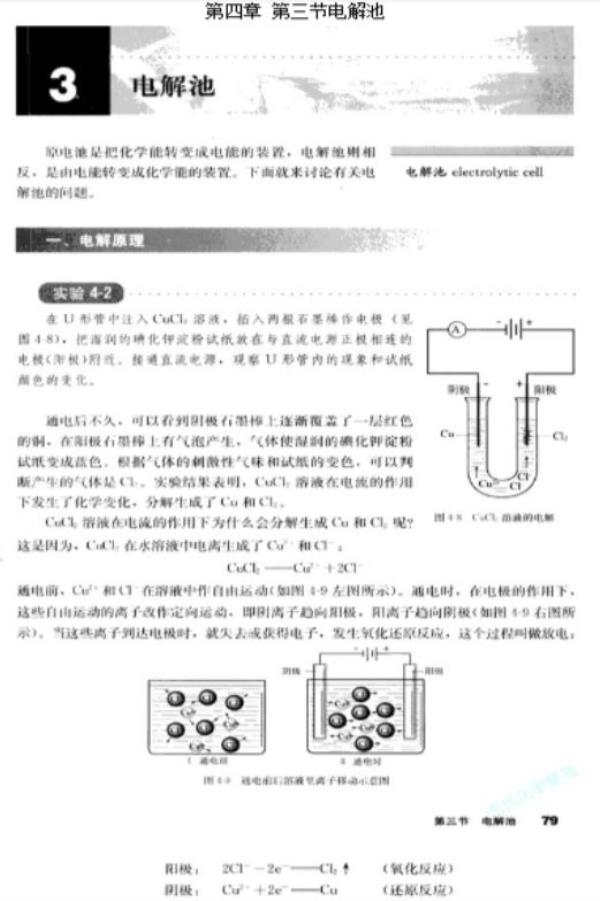
3、基本要求:
(1)试讲时间10分钟
(2)教学过程有适当提问,师生互动
(3)教学过程中需要教具的,进行演示即可
教学设计
一、导入
师:上节课我们学习了原电池的有关知识,请大家回忆,构成原电池的条件是什么?生:(思考)构成原电池的条件:活泼性不同的两个电极;电解质溶液;生:形成闭合电路:自发氧化还原反应.
二、新课讲授
师:[投影显示]如下图所示。大家观察实验现象,并回答:①电流表指针的变化。②碳棒上有什么变化?在两极发生了什么反应?
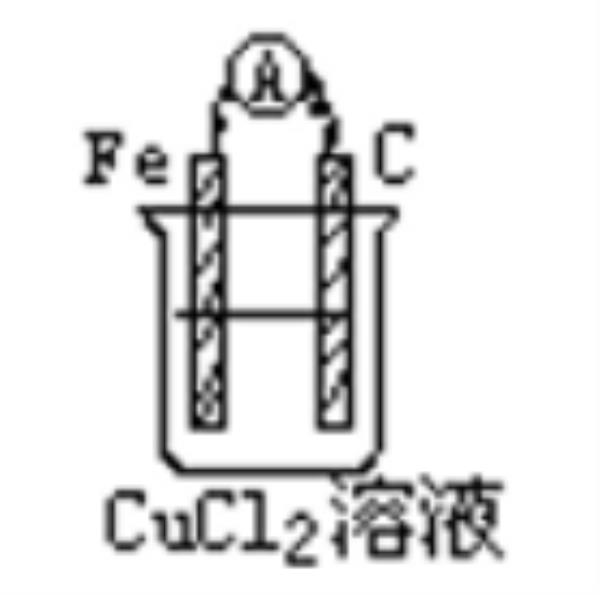
(生观察现象)生:1.电流表的指针发生偏移:生:2.碳棒上有红色物质生成.
师:请大家是这写出电极反应.生:铁为负极,碳棒为正极。
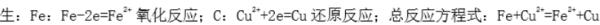
师:这里设计了三个实验,请大家分组实验并观察实验现象,准确记录实验现象,汇报实验结果.[投影显示]1.将两根碳棒分别插入装有 CuClz溶液的小烧杯中,浸一会,取出碳棒观察碳棒表面现象(图1);2.用导线连接碳棒后,再浸入CuCl2溶液一会儿,取出碳棒,观察碳棒表面变化(图2);3.浸入CuClz溶液中的两根碳棒,分别跟直流电源的正极和负极相连接,接通一段时间后,观察两极上的现象并用湿润的KI-淀粉试纸检验所生成的气体(图3).
师:在此过程中请大家一定要操作规范,注意安全。生:前两个实验碳棒上没有明显变化;生:第三个实验通电一会儿发现,与电源负极相连的一端的碳棒上有红色固体物质析出:生:与电源正极相连的一端碳棒上有使湿润的淀粉-KI 试纸变蓝的气体生成。全部生:分析整理作出判断。红色物质为铜,黄绿色使湿润淀粉-KI 试纸变蓝的气体为氯气。阳极产物——氯气(Cl2):阴极产物——铜(Cu)
师:为什么会有这样的结果?[提示]讨论提纲[投影显示]1.通电前溶液中存在哪些离子?这些离子是如何运动的?2.接通直流电后,原来的离子运动发生了怎样的改变?3.有关离子在两极发生了什么样的反应?
生:(讨论分析)

师:[总结板书]

[概括]通俗记法,利用谐音。阳(极)一氧(化反应)
师:在电解过程中,电子是如何形成闭合回路的?大家请看看课本第64页,归纳电子流动方向.生:电源负极一电解池阴极一电解质溶液一电解池阳极一电源正极
师:非常正确,我们一来总结一下.
师生:电子的方向与电流的方向相反从电源负极流出,流向电解池的阴极,阴极附近的 Cu在阴极得电子被还原为铜,溶液中的阴阳离子定向移动,阳极附近的CI在阳极失电子被氧化为氯原子。氯原子结合形成氯气分子,失去的电子从阳极流回电源的正极,从而形成了闭合电路.
师:电解质溶液的导电与溶液的电离有什么关系?生:先有电离,后有电解。电离不需要通电,电解建立在电离的基础上。
师:现在大家一起来完成投影显示的表格。生:(每位学生完成一项,共同填好此表。)
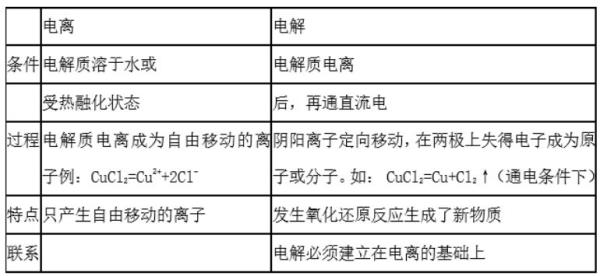
师:(视学生回答情况给予表扬或完善)。
师生:电解质溶液的导电过程就是它的电解过程,这一过程能够进行的前提是溶液中有自由移动的离子,也就是说,先电离,在外加直流电源的条件下,才能发生电解。
师:金属导电与电解质溶液导电有什么不同?
生:思考
师:[提示]从做定向移动的微粒有什么不同,和有没有发生化学变化来比较。
生:金属导电靠自由电子的定向移动,移动过程不发生化学变化。电解质溶液导电是阴阳离子的定向移动,在两极发生氧化还原反应。
师:在电解中我们经常使用的电极有两种,一种是惰性电极,就是电极本身不参加化学变化,如石墨、铂电极等。还有另外一种是金属做电极,它们在电解中本身发生了化学变化,我们在下节课继续学习。
三、巩固练习
标明下列装置中电解质的阴阳极,写出电极反应的化学方程式,并判断是氧化反应,还是还原反应?
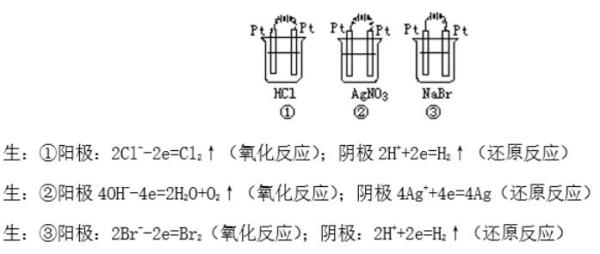
四、课堂小结
师:让我们一起来回忆一下这节课我都学习了哪些内容。生:电解的概念及电解的原理,会判断电解池的阴阳两极,写电极反应方程式,判断所发生的氧化还原反应.
五,布置作业
1.复习课本第62~65页第一段.
2.预习电解原理的应用.
3.列表比较原电池和电解池的异同。
[提示:从电极的确定及名称,两极所发生的反应,能量的转换等几项考虑。
相关文章
版权声明:部分内容为互联网整合,文中观点不代表本站立场。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容,请发送邮件举报,一经查实,本站将立刻删除。
为您推荐
精品文章
热门推荐